Контакт:Эррол Чжоу (мистер)
Тел: плюс 86-551-65523315
Мобильный/WhatsApp: плюс 86 17705606359
QQ:196299583
Скайп:lucytoday@hotmail.com
Электронная почта:sales@homesunshinepharma.com
Добавлять:1002, здание Хуанмао, № 105, улица Мэнчэн, город Хэфэй, 230061, Китай
Компания MEI Pharma и ее глобальный партнер Kyowa Kirin недавно обнародовали последние данные о пероральном селективном ингибиторе фосфатидилинозитол-3-киназы дельта (PI3K delta) занделисиб (ME-401) для лечения злокачественных опухолей B-клеток.
Результаты показали, что у пациентов с рецидивирующей или рефрактерной фолликулярной лимфомой (FL), у которых наблюдалось прогрессирование заболевания (POD24) в течение 24 месяцев после получения химиотерапевтического лечения первой линии, занделисиб (с ритуксимабом и без него). 82%, а ЧОО достигала 93% у пациентов без POD24. Кроме того, комбинированная терапия занделисибом и занубрутинибом (Зебутиниб, ингибитор BeiGene BTK) позволила достичь 100% ЧОО при лечении рецидивирующих или рефрактерных В-клеточных злокачественных новообразований с оптимизированным режимом дозирования. Подробные данные будут объявлены на ежегодном собрании Американского общества клинической онкологии (ASCO) 2021 года, которое состоится в начале июня этого года.
Занделисиб (ME-401) - исследуемый пероральный ингибитор фосфатидилинозитол-3-киназы (PI3K) дельта. Ингибиторы PI3Kδ обычно сверхэкспрессируются в раковых клетках и играют ключевую роль в пролиферации и выживании гематологических опухолей. Занделисиб проявляет высокую селективность в отношении подтипов PI3Kδ и обладает лекарственными свойствами, отличными от других ингибиторов PI3Kδ. Этот препарат может стать лучшим в своем классе ингибитором PI3Kδ. Его клинические характеристики указывают на то, что в качестве монотерапии или в сочетании с другими противораковыми препаратами он имеет возможность вылечить ряд В-клеточных злокачественных новообразований. В настоящее время MEI изучает занделисиб для лечения пациентов с различными В-клеточными злокачественными новообразованиями. В 2020 году FDA США предоставило занделисибу статус ускоренного приема (BTD).
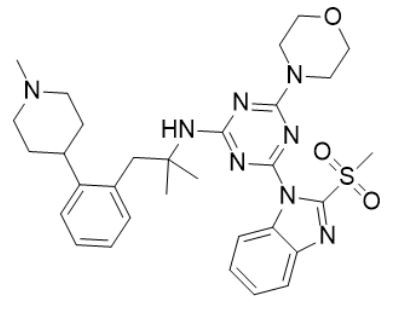
Молекулярная структура занделисиба (источник изображения: invivochem.com)
Последние данные фазы 1b исследования занделисиба в лечении р / р ФЛ:
Текущее клиническое исследование фазы 1b - это открытое исследование с несколькими группами по оптимизации дозы, в котором в настоящее время используется занделисиб в качестве монотерапии и в сочетании с другими методами лечения злокачественных новообразований r / r B-клеток. Данные, представленные в этом отчете, относятся к пациентам с прерывистым режимом (прерывистый режим, IS): 60 мг один раз в день в течение 2 циклов (28 дней / цикл), а затем прерывистое введение, то есть каждый цикл (28 дней / цикл). ) 60 мг 1 раз в день в течение первых 7 дней. В общей сложности 37 пациентов с р / р ФЛ получали периодический режим дозирования занделисиба либо в виде монотерапии, либо в комбинации с ритуксимабом. Среди 37 пациентов с r / r FL у 22 был POD24. POD24 является мощным средством прогнозирования общей выживаемости FL.
Данные об общей частоте ответа (ЧОО): среди 37 пациентов с р / р ФЛ ЧОО составляла 87%, а частота полного ответа (ПО) - 27%. ЧОО составила 82% у пациентов с POD24 и 93% у пациентов без POD24. CR составлял 18% у пациентов с POD24 и 40% у пациентов без POD24.
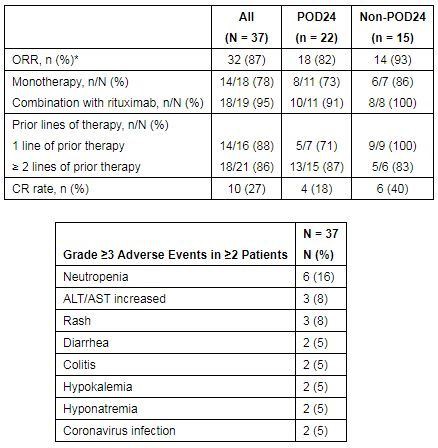
Клинические данные занделисиба в лечении ФЛ
Продолжительность ремиссии (DOR): медиана DOR пациентов с POD24 и без POD24 еще не достигнута. Среднее время наблюдения за пациентами с POD24 составляло 15,8 месяцев (диапазон: 5,6-33,1), а средняя продолжительность ремиссии у пациентов без POD24 составляла 17 месяцев (диапазон: 1,2-28,6).
Выживаемость без прогрессирования (ВБП): средняя ВБП пациентов с ПОБ 24 составляет 12,5 месяцев, а средняя ВБП пациентов без ПОБ еще не достигнута. Среднее время наблюдения за пациентами с POD24 составляло 19,4 месяца (диапазон: 1,8-36,5), а средняя продолжительность ремиссии у пациентов без POD24 составляла 18,2 месяца (диапазон: 3,0-30,4).
Побочные эффекты: Занделисиб обычно хорошо переносится. Не было различий в побочных эффектах между группой POD24 и группой без POD24. Частота прекращения лечения из-за нежелательных явлений (ПВНЯ) во время лечения составила 8% (n=3).
Доктор Джон Пагель, исследователь исследования занделисиба и директор по гематологическим злокачественным новообразованиям Шведского онкологического центра, сказал: «Пациенты с рецидивирующей или рефрактерной фолликулярной лимфомой (r / r FL) прогрессируют в течение 24 месяцев после химиоиммунотерапии первой линии (POD24. ), по сравнению с пациентами с r / r FL, у которых возник рецидив через 24 месяца (без POD24), долгосрочный прогноз плохой и представляет собой высокую потребность в новых вариантах лечения. Полученные сегодня положительные результаты указывают на то, что занделисиб потенциально может представлять собой группу высокого риска для пациентов с р / р FL, что является новым вариантом лечения."
Последние данные фазы 1b исследования занделисиба в сочетании с занубрутинибом при лечении В-клеточных злокачественных опухолей:
Текущее клиническое исследование фазы 1b - это открытое исследование с несколькими группами по оптимизации дозы, в котором в настоящее время используется занделисиб в качестве монотерапии и в сочетании с другими методами лечения злокачественных новообразований r / r B-клеток. Данные в этом отчете относятся к 20 пациентам, получавшим комбинированную терапию занделисибом и занубрутинибом. Были изучены два режима дозирования: группа А получала занделисиб 60 мг один раз в день в течение 8 недель, затем первые 7 дней каждого цикла (28 дней / цикл), занубрутиниб в дозе 160 мг перорально два раза в день. Группа B получала 60 мг занделисиба один раз в день, начиная с первого цикла первых 7 дней каждого цикла (28 дней / цикл), а доза занубрутиниба составляла 80 мг перорально два раза в день. 7 пациентов были включены в группу A (1 FL, 3 CLL, 1 MZL, 1 MCL, 1 DLBCL / HGBCL) и 13 пациентов в группу B (7 FL, 2 CLL, 1 случай MZL, 3 случая DLBCL / HGBCL). Лечение до прогрессирования заболевания, непереносимости или отзыва информированного согласия.

Клинические данные занделисиба в лечении В-клеточных злокачественных новообразований
Общая частота ответа (ЧОО): среди всех оцениваемых r / r индолентных В-клеточных злокачественных новообразований и пациентов с ХЛЛ ЧОО составляет 100%. Однако 2 случая DLBCL / HGBCL не показали ремиссии. Ремиссия является продолжительной, со средним сроком наблюдения 6,6 месяцев (0,6–21,3), и большинство пациентов с ремиссией все еще получают лечение.
Среди 8 пациентов с ФЛ 2 (25%) достигли полной ремиссии или полной ремиссии с неполным восстановлением количества клеток крови (CR / CRi=25%), а 2 из 5 случаев CLL (40%) достигли CR / CRi. .
В завершенной части исследования занделисиб 60 мг один раз в день вводили из первого цикла (28 дней / цикл) в первые 7 дней каждого цикла (28 дней / цикл) в сочетании сзанубрутинибдоза 80 мг перорально 2 раза в сутки. Этот график дозирования предназначен для всех В-клеток. Злокачественные опухоли переносятся хорошо. Комбинация лекарств в оптимизированном режиме дозирования группы B не вызовет дополнительной токсичности для каждого лекарства в отдельности.
Исследователь и доцент Гарвардской медицинской школы и онкологического центра Массачусетской больницы общего профиля Джейкоб Сумераи, доктор медицины, сказал:" Данные, представленные сегодня о комбинированном применении занделисиба и занубрутиниба, обнадеживают как с точки зрения начальной безопасности, так и эффективность. И поддержать расширение оценки пероральных комбинированных препаратов для лечения различных В-клеточных злокачественных новообразований."